인더뉴스 김진희 기자ㅣ 식품의약품안전처가 경피용(도장형) 건조비씨지(BCG)백신(일본균주)에서 기준 초과 비소가 검출됐다는 일본 후생성 정보에 따라 국내 해당 제품에 대한 회수 조치를 내렸다.
7일 식약처에 따르면 일본 후생성이 결핵 예방을 위해 1세 미만 영아에 접종하는 BCG 백신의 첨부용액(생리식염수주사용제)에서 기준을 초과한 비소가 검출돼 출하를 정지했다는 발표에 따라 해당 제품을 회수키로 했다.
회수 대상은 견피용(도장형) 건조비씨지(BCG)백신(일본균주)으로 일본비씨지가 제조하고 한국백신상사가 수입하고 있는 제품이다.
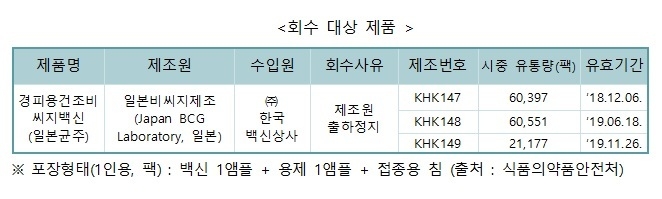
시중에 유통된 제품은 제조번호 KHK147(유효기간 2018년 12월 6일) 6만 397팩, KHK148(유효기간 2019년 6월18일) 6만 551팩, KHK149(유효기간 2018년 11월 26일) 2만 1177팩이다. 1팩당 백신 1앰플과 용제 1앰플, 접종용 침이 포장돼 있다.
식약처에 따르면 일본 후생성은 백신이 아닌 첨부용제(생리식염수액)가 일본약전 비소기준을 초과했다고 발표했다.
하지만 일본 국립의약품식품위생연구소의 건강영향평가 결과, 함유된 비소로 인한 안전성에는 문제가 없는 것으로 나타났고, 이에 일본에서는 회수없이 제조소 출하만 정지됐다.
반면 식약처는 해당 제품에 대해 회수 조치를 결정했다. 식약처 관계자는 “일본 후생성 조치를 면밀히 검토하되, 국내에서는 피내용(주사형) 건조비씨지(BCG)백신이 대체품으로 있는 상황을 고려해 우선 해당 제품에 대해 회수조치한다“고 설명했다.
또한, “회수조치에 따른 경피용(도장형) 비씨지백신 공급 차질을 최소화하기 위해 추가적인 대책을 신속하게 마련하도록 하겠다“고 덧붙였다.
ICH Q3D 가이드라인에 따르면 비소(주사) 1일 최대 허용량은 1.5㎍/일(5㎏)이다. 첨부용제 최대 함유 비소 0.039㎍(0.26ppm)투여시 1일 허용량의 1/38 수준이며, 가이드라인의 1일 허용량은 평생기준이나 BCG백신은 평생 1회만 접종하고 있다.
한편 질병관리본부는 국가결핵예방접종용 백신인 피내용(주사형) BCG백신은 국내 충분히 공급 중이라고 발표했다. 내년 상반기까지 40만명 이상이 접종 가능한 2만 9322바이알을 재고로 보유하고 4만 4000바이알을 예상 공급 물량으로 확보하고 있다는 것.
다만, 피내용(주사형) BCG접종을 제공할 전국 보건소와 지정의료기관이 제한돼 불편할 수 있다고 전했다. 피내용(주사형) BCG 백신 접종이 가능한 지정의료기관은 372개소며, 예방접종도우미 홈페이지에서 확인 가능하다.
질병관리본부는 “영유아 보호자들은 가까운보건소 또는 지정의료기관을 사전확인 후 방문해 줄 것“을 당부했다.



















